国家药监局综合司公开征求《关于做好第三批实施医疗器械唯一标识工作的公告(征求意见稿)》意见
为进一步贯彻落实《医疗器械监督管理条例》《国务院办公厅关于印发治理高值医用耗材改革方案的通知》和国务院深化医药卫生体制改革有关重点工作任务,推进医疗器械唯一标识在监管、医疗、医保等领域的衔接应用,国家药监局组织起草了《关于做好第三批实施医疗器械唯一标识工作的公告(征求意见稿)》(见附件),现公开征求意见。
请将修改意见和建议于2022年12月30日前反馈至电子邮箱:mdct@nmpa.gov.cn,邮件标题注明“UDI第三批实施”。
联系人及电话:董谦,010-88330608。
附件:关于做好第三批实施医疗器械唯一标识工作的公告(征求意见稿)
附件:
关于做好第三批实施医疗器械唯一标识工作的公告
(征求意见稿)
附:
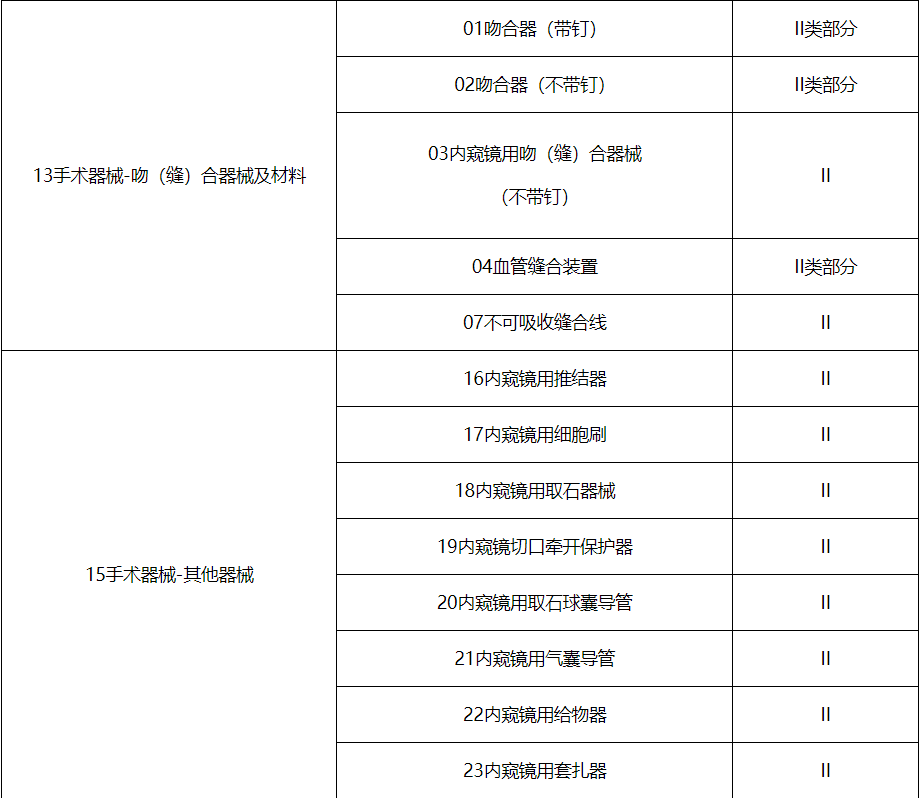
第三批实施医疗器械唯一标识的产品目录








一级产品类别 | 二级产品类别 | 管理类别 |
03光治疗设备 | 01激光治疗设备 | II类部分 |
02光动力激光治疗设备 | II类部分 | |
04强脉冲光治疗设备 | II | |
05红光治疗设备 | II | |
06蓝光治疗设备 | II |
一级产品类别 | 二级产品类别 | 管理类别 |
03血液净化及腹膜透析设备 | 06腹膜透析设备 | II |
04血液净化及腹膜透析器具 | 04腹膜透析器具 | II类部分 |
一级产品类别 | 二级产品类别 | 管理类别 |
01心脏节律管理设备 | 10起搏系统分析设备 | II |
11心脏节律管理程控设备 | II | |
12连接器套筒 | II | |
02神经调控设备 | 07测试刺激器 | II |
08测试延伸导线 | II | |
09神经调控程控设备 | II | |
03辅助位听觉设备 | 02体外声音处理器 | II |
03辅助位听觉调控设备 | II | |
04其他 | 01植入式心脏收缩力 调节设备 | II类部分 |
一级产品类别 | 二级产品类别 | 管理类别 |
01注射、穿刺器械 | 01注射泵 | II类部分 |
04笔式注射器 | II | |
07注射器辅助推动装置 | II类部分 | |
08穿刺器械 | II | |
09活检针 | II | |
02血管内输液器械 | 01输液泵 | II类部分 |
12药液用转移、配药器具 | II | |
05非血管内导(插)管 | 02经鼻肠营养导管 | II |
03导尿管 | II类部分 | |
04直肠管(肛门管) | II类部分 | |
05输尿管支架 | II类部分 | |
06引流导管 | II | |
07扩张导管 | II | |
08造影导管 | II | |
09测压导管 | II | |
06与非血管内导管配套用体外器械 | 01颅脑外引流收集装置 | II |
02胸腔引流装置 | II | |
05负压引流海绵 | II类部分 | |
06负压引流封闭膜 | II | |
12造口、疤痕护理用品 | 02疤痕修复材料 | II |
14医护人员防护用品 | 01防护口罩 | II |
02防护服 | II |
一级产品类别 | 二级产品类别 | 管理类别 |
03视光设备和器具 | 03视觉治疗设备 | II |
04眼科测量诊断设备 和器具 | 01眼科激光诊断设备 | II类部分 |
05眼科治疗和手术设备、辅助器具 | 04眼科冷冻治疗设备 | II |
06眼科治疗和手术辅助器具 | II类部分 | |
07眼科植入物及辅助器械 | 14义眼片 | II类部分 |
15人工晶状体、人工玻璃体 植入器械 | II类部分 | |
16 囊袋张力环植入器械 | II类部分 |
一级产品类别 | 二级产品类别 | 管理类别 |
01妇产科手术器械 | 05妇产科用扩张器、牵开器 | II类部分 |
10子宫输卵管造影、输卵管 通液器械 | II类部分 | |
04妇产科治疗器械 | 02妇科假体器械 | II类部分 |
07辅助生殖器械 | 01辅助生殖导管 | II |
02辅助生殖穿刺取卵/精针 | II | |
03辅助生殖微型工具 | II |
一级产品类别 | 二级产品类别 | 管理类别 |
01认知言语视听障碍康复设备 | 07助听器 | II |
一级产品类别 | 二级产品类别 | 管理类别 |
01血液学分析设备 | 02血细胞分析仪器 | II |
11采样设备和器具 | 04静脉血样采血管 | II |



